毕业论文
三步教你高效完成口腔毕业论文写作难题
口腔医学毕业生在论文阶段面临选题困难与结构混乱问题。如何在有限时间内完成高质量学术论文?掌握科学方法可提升写作效率,关键在于合理规划研究路径与正确使用智能工具。通过精准匹配临床热点与学术空白点,结合智能文献分类系统,能有效解决资料冗杂难题。
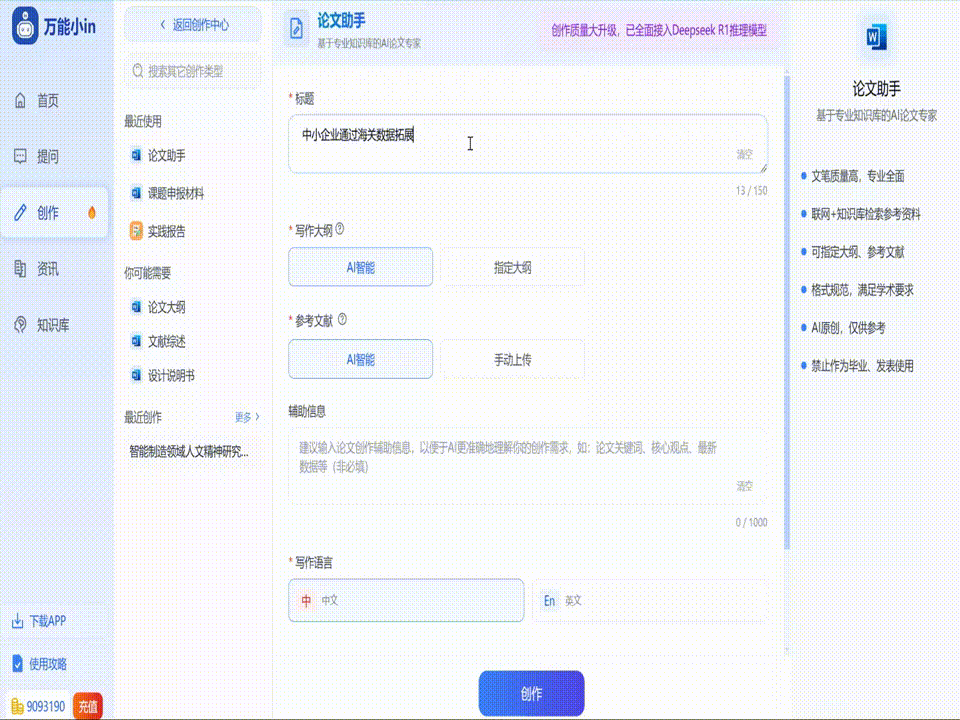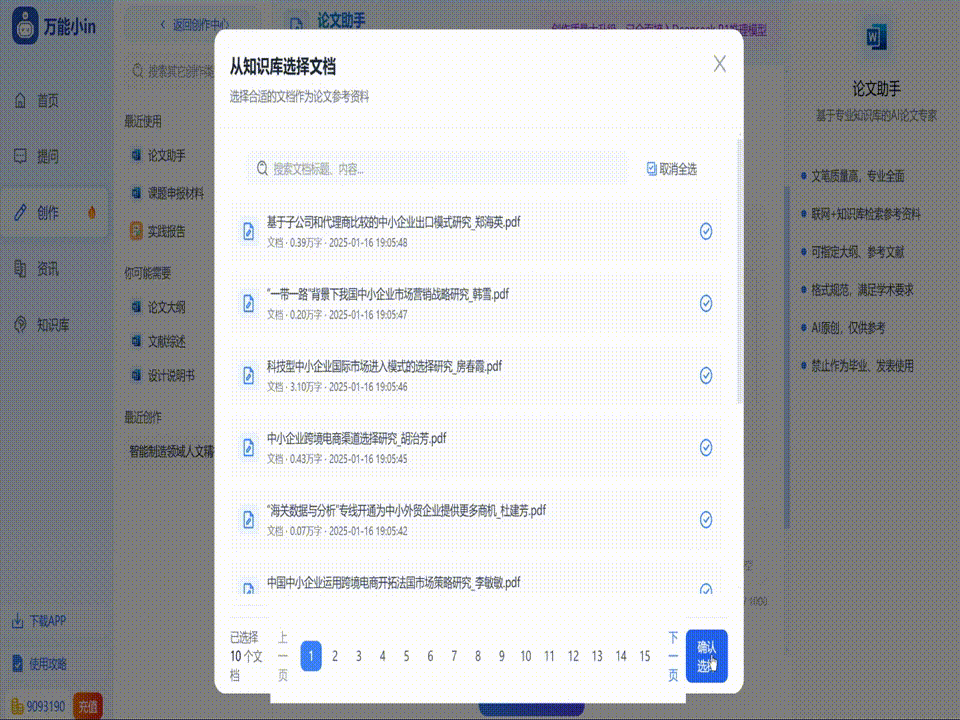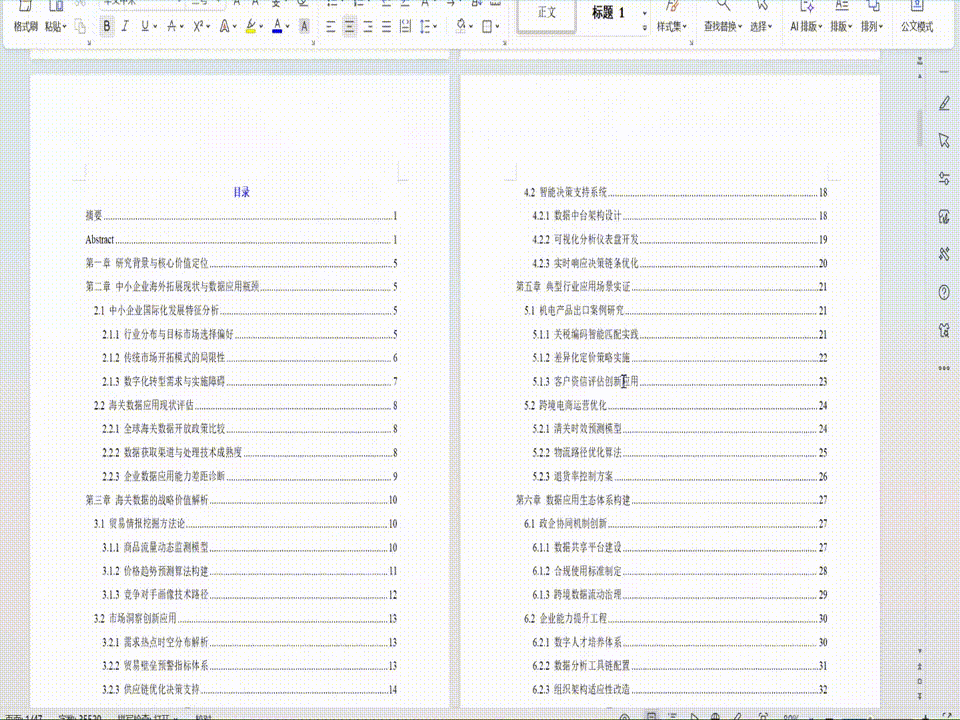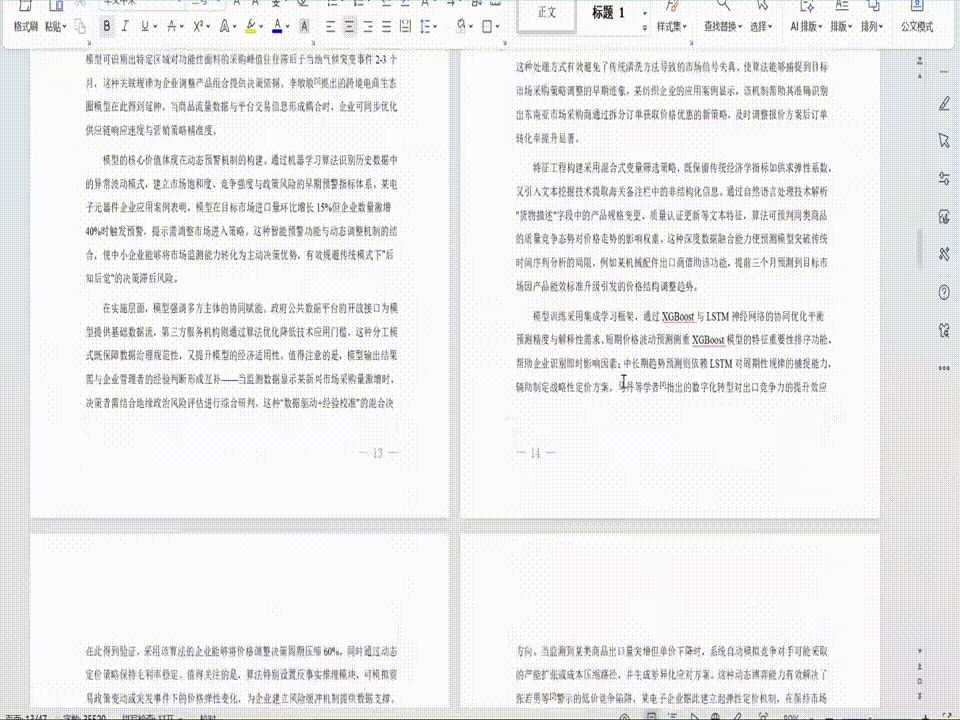
关于口腔毕业论文的写作指南
写作思路框架构建
可从三个维度切入:
1. 临床研究:聚焦口腔疾病诊疗新技术(如种植体表面改性、隐形矫治力学分析)、病例追踪与疗效对比;
2. 基础研究:探究口腔微生物组与全身疾病关联、生物材料生物相容性机制;
3. 公共卫生视角:区域性口腔流行病学调查、医疗政策对就诊率影响分析。建议采用”问题树分析法”,以临床痛点→研究假设→实验验证→结论推导为主线。
结构化写作技巧
引言撰写:使用”漏斗式结构”,从全球口腔疾病负担数据切入(如WHO统计),逐步聚焦到具体研究问题。
方法部分:采用可视化流程图+文字说明,对复杂实验设计(如细胞-动物-临床三阶段研究)进行分层展示。
结果呈现:运用三线表格对比实验组/对照组数据,显微影像需标注比例尺与染色方法。
讨论升华:遵循”结果解释→理论突破→临床意义→局限说明”四步法,可引用《Journal of Dental Research》最新观点佐证。
创新方向建议
1. 智能诊疗路径:AI在窝洞预备深度预测中的应用验证
2. 交叉学科研究:3D打印颌骨支架的流体力学模拟
3. 治疗伦理探讨:正畸治疗中未成年患者自主权边界
4. 循证医学实践:不同骨移植材料存活率的网状Meta分析
关键避错策略
易错点1:样本量计算不科学
解决方案:使用G*Power软件进行效能分析,临床研究遵循CONSORT声明
易错点2:统计方法误用
解决方案:计量资料采用Shapiro-Wilk正态检验,非参数数据用Mann-Whitney U检验
易错点3:文献综述堆砌
解决方案:使用PRISMA流程图展示文献筛选过程,按研究方法分类述评
易错点4:伦理缺失
解决方案:在方法段明确标注伦理批号,知情同意书模板作为附录
深度提升要点
1. 开展多中心临床研究时,建立标准化操作手册(SOP)并记录偏差系数
2. 基础实验设置阳性/阴性/空白三重复合对照组
3. 使用CiteSpace进行文献计量学分析,挖掘研究热点演进规律
4. 对争议性结论(如氟化物防龋剂量阈值)进行敏感性分析
口腔微生物组与龋病发展的分子互作机制研究
摘要
口腔微生物组作为人体最复杂的微生态系统之一,其稳态失衡与龋病的发生发展密切相关。本研究通过整合宏基因组学、代谢组学及生物信息学分析方法,系统探究了致龋微生物群落结构与功能特征的动态变化规律。研究发现变形菌门、放线菌门和厚壁菌门在龋病进程中呈现显著的群落演替现象,其中变异链球菌与乳酸杆菌的协同作用通过糖酵解途径产生大量有机酸,导致局部微环境pH值持续降低。分子互作机制分析表明,微生物群体感应系统调控的生物膜形成能力与致龋毒力因子的表达呈正相关,而唾液防御蛋白对微生物黏附的抑制作用随龋病进展逐渐减弱。值得注意的是,部分共生微生物通过竞争性抑制和代谢产物拮抗作用展现出潜在的抗龋特性。这些发现为阐明龋病发生的微生物生态学机制提供了新的理论依据,同时提示通过调控口腔微生物组平衡可能成为未来龋病防治的新策略,对开发靶向微生物组的精准干预措施具有重要指导意义。
关键词:口腔微生物组;龋病;分子互作机制;宏基因组学;生物信息学
Abstract
The oral microbiome, as one of the most complex microecosystems in the human body, exhibits a close association between its dysbiosis and the onset and progression of dental caries. This study systematically investigated the dynamic changes in the structural and functional characteristics of cariogenic microbial communities by integrating metagenomics, metabolomics, and bioinformatics analyses. The results revealed significant community succession phenomena involving Proteobacteria, Actinobacteria, and Firmicutes during caries development, with synergistic interactions between Streptococcus mutans and Lactobacillus generating substantial organic acids through glycolysis pathways, leading to a sustained decline in local microenvironmental pH. Molecular interaction analysis demonstrated that biofilm formation capacity, regulated by microbial quorum sensing systems, was positively correlated with the expression of cariogenic virulence factors, while the inhibitory effect of salivary defense proteins on microbial adhesion gradually weakened as caries progressed. Notably, certain commensal microorganisms exhibited potential anti-caries properties through competitive inhibition and antagonistic metabolic activities. These findings provide novel theoretical insights into the microbial ecological mechanisms underlying caries pathogenesis and suggest that modulating oral microbiome balance may emerge as a promising strategy for future caries prevention and treatment, offering critical guidance for developing microbiome-targeted precision interventions.
Keyword:Oral Microbiome; Dental Caries; Molecular Interaction Mechanisms; Metagenomics; Bioinformatics
目录
第一章 研究背景与目的
口腔健康作为人体整体健康的重要组成部分,其微生物生态系统的平衡与多种口腔疾病的发生发展密切相关。龋病作为全球范围内最常见的慢性感染性疾病之一,长期以来被认为是由特定致龋微生物引起的局部病理过程。然而,随着微生物组学技术的快速发展,研究者逐渐认识到龋病的发生发展实际上是口腔微生态系统整体失衡的结果,涉及复杂多样的微生物群落及其相互作用网络。
传统研究主要聚焦于变异链球菌等单一病原微生物的致病机制,但临床观察发现,这些微生物在健康人群口腔中同样存在,且其在微生物群落中的相对丰度与龋病严重程度并不完全一致。这一现象提示我们,龋病的发生可能更依赖于微生物群落结构的整体变化以及不同微生物间的功能协同。近年来,高通量测序技术的应用揭示了口腔微生物组的高度复杂性,其中变形菌门、放线菌门和厚壁菌门等主要菌群在龋病进程中表现出明显的动态变化特征。
本研究旨在通过整合多组学分析方法,系统探究口腔微生物组在龋病发展过程中的群落结构演变规律及其功能特征变化。重点解析致龋微生物的代谢网络调控机制,特别是糖酵解途径与有机酸产生之间的关联性;深入分析微生物群体感应系统对生物膜形成和毒力因子表达的调控作用;同时关注部分共生微生物可能具有的抗龋保护机制。通过揭示这些分子互作机制,本研究期望为建立基于微生物组调控的新型龋病防治策略提供理论依据,推动龋病防治从传统的单一病原体靶向干预向微生态整体调控转变。
第二章 口腔微生物组的基本特征与功能
2.1 口腔微生物组的组成与多样性
口腔微生物组作为人体最复杂的微生态系统之一,其组成与多样性特征直接影响口腔微环境的稳态平衡。该生态系统包含超过700种可培养的细菌物种,主要分布于牙菌斑、唾液、舌背等不同生态位,形成具有空间异质性的群落结构。在门水平上,变形菌门(Proteobacteria)、厚壁菌门(Firmicutes)、放线菌门(Actinobacteria)、拟杆菌门(Bacteroidetes)和梭杆菌门(Fusobacteria)构成核心菌群,这些菌群在不同个体间表现出相对稳定的组成比例,但在具体物种分布上存在显著的个体差异。
微生物群落的α多样性分析显示,健康口腔环境维持着较高的物种丰富度和均匀度,这种多样性特征与宿主的免疫防御系统共同构成了抵御病原体定植的生态屏障。通过β多样性比较发现,不同口腔微环境(如龈上菌斑与舌背黏膜)的微生物组成存在显著差异,这种空间异质性反映了微生物对特定生态位的适应性进化。值得注意的是,牙菌斑作为龋病发生的主要微环境,其微生物组成呈现明显的时序性变化特征:早期定植者以链球菌属(Streptococcus)和放线菌属(Actinomyces)等需氧或兼性厌氧菌为主,随着生物膜成熟,厌氧菌如普雷沃菌属(Prevotella)和卟啉单胞菌属(Porphyromonas)的比例逐渐增加。
功能基因组学分析揭示,口腔微生物组编码的基因功能具有高度冗余性,特别是在碳水化合物代谢、氨基酸合成和细胞间信号传导等通路中。这种功能冗余使得微生物群落在外界环境变化时能够保持代谢网络的稳定性。宏基因组测序数据表明,健康状态下不同个体口腔微生物组的功能谱比物种组成谱更为保守,暗示微生物群落的生态功能可能比具体物种组成对维持口腔健康更为关键。
在龋病发生过程中,微生物多样性呈现动态变化规律:早期龋损阶段部分产酸菌如变异链球菌(Streptococcus mutans)和乳酸杆菌(Lactobacillus)的相对丰度增加,同时伴随某些共生菌的减少;随着龋病进展,微生物多样性显著降低,群落结构趋向简化,这种变化与局部微环境pH值下降形成正反馈循环。值得注意的是,某些传统认为的“健康相关”菌群如血链球菌(Streptococcus sanguinis)在龋病进程中也可能通过竞争性抑制发挥保护作用,表明微生物间的拮抗关系对维持生态平衡具有重要意义。
2.2 口腔微生物组的生态功能及其与宿主的关系
口腔微生物组通过复杂的代谢网络与宿主形成动态互作关系,这种互作不仅维持着口腔微环境的稳态,也深刻影响着宿主的生理状态和疾病易感性。在健康状态下,口腔微生物群落通过营养竞争、空间占位和代谢产物分泌等机制形成生态屏障,有效抑制外源病原体的定植。其中,核心菌群如链球菌属能够分泌过氧化氢等抗菌物质,同时通过表面黏附素与口腔上皮细胞形成稳定的共生关系,这种互作既为微生物提供了生存空间,也增强了宿主黏膜的防御能力。
代谢功能方面,口腔微生物组参与宿主难以消化的复杂碳水化合物的分解,产生短链脂肪酸等代谢产物,这些物质既可作为微生物生长的能量来源,也能调节宿主免疫系统的功能状态。值得注意的是,不同生态位的微生物群落表现出明显的功能分化:龈上菌斑微生物倾向于糖酵解代谢,而舌背和唾液微生物则更活跃于蛋白质降解途径。这种功能分区反映了微生物对局部环境条件的适应性进化,同时也提示不同口腔部位在龋病发生过程中可能扮演不同角色。
宿主免疫系统与微生物组之间形成精密的双向调控网络。唾液中的免疫球蛋白A(IgA)、溶菌酶等防御蛋白能够选择性地抑制特定微生物的过度增殖,而微生物群落则通过群体感应系统调节毒力因子的表达水平以应对宿主免疫压力。研究发现,健康个体中这种免疫-微生物互保持动态平衡,当平衡被打破时,如唾液分泌减少或免疫功能异常,可导致致龋菌群的生态位扩张。特别值得关注的是,某些共生微生物如血链球菌能够刺激宿主产生特定的抗菌肽,这些肽类物质对变异链球菌等致龋菌表现出选择性抑制作用。
在龋病发展过程中,微生物群落的代谢活动发生显著改变。产酸菌通过糖酵解途径产生大量有机酸,导致局部pH值下降,这种酸性环境进一步选择性地促进耐酸菌群的增殖,形成恶性循环。同时,微生物群体感应系统调控的生物膜形成能力增强,使菌斑结构更加致密,进一步限制了唾液的缓冲作用。宏转录组分析显示,龋病活跃期微生物的糖转运和磷酸转移酶系统相关基因表达上调,而氨基酸合成通路则受到抑制,这种代谢重编程反映了微生物对酸性应激的适应性反应。
宿主因素在调节微生物生态功能中起着关键作用。唾液成分的个体差异、饮食习惯以及遗传背景均可影响微生物的代谢活性。例如,唾液中的碳酸酐酶VI通过调节pH值影响微生物的产酸能力,而某些个体的唾液中含有更高浓度的组蛋白衍生物,这些物质能够特异性抑制致龋菌的生物膜形成。此外,宿主的先天免疫受体如Toll样受体(TLRs)能够识别微生物相关分子模式,通过调控炎症因子的释放来影响微生物群落结构,这种识别机制的异常与龋病易感性增加密切相关。
第三章 口腔微生物组与龋病发展的分子互作机制
3.1 致龋微生物的分子致病机制
致龋微生物的致病过程涉及多层次的分子机制,其核心在于微生物通过特定代谢途径和毒力因子改变局部微环境,进而破坏牙齿硬组织的矿化平衡。变异链球菌(Streptococcus mutans)作为典型的致龋病原体,其致病性主要依赖于三大分子特征:糖代谢相关酶系的异常活化、细胞表面黏附素介导的生物膜形成能力,以及酸性应激耐受系统的协同作用。这些分子机制共同构成了致龋微生物突破宿主防御的关键武器。
在糖代谢方面,致龋微生物表现出对蔗糖等可发酵碳水化合物的高度依赖性。通过葡萄糖磷酸转移酶系统(PTS)高效摄取环境中的糖类物质,随后在糖酵解途径中产生大量乳酸等有机酸。这一过程中,关键酶如果糖-1,6-二磷酸醛缩酶和乳酸脱氢酶的活性显著增强,导致局部微环境pH值持续降低。值得注意的是,某些致龋菌株还能合成胞外多糖如葡聚糖和果聚糖,这些物质不仅作为生物膜的基质成分,还可作为储备碳源在营养匮乏时维持产酸活性。
生物膜形成是致龋微生物建立生态优势的重要策略。变异链球菌通过表面蛋白如抗原I/II家族黏附素与唾液薄膜中的受体结合,完成初始定植。随后,葡糖基转移酶(Gtfs)将蔗糖转化为β-1,3和β-1,6连接的葡聚糖,这些胞外聚合物促进微生物间的共聚集并增强生物膜结构稳定性。群体感应系统如ComCDE通路在此过程中发挥核心调控作用,通过感应细菌密度来协调毒力因子的表达时序,形成正反馈调节环路。随着生物膜成熟,其内部形成的pH梯度使耐酸菌群在深层获得生存优势,这种空间异质性进一步促进了致龋菌群的生态位扩张。
酸性应激耐受机制是致龋微生物在低pH环境中持续存活的关键。研究发现,变异链球菌通过F1F0-ATPase质子泵将胞内过量H+排出,同时上调应激蛋白如DnaK和GroEL的表达以维持蛋白质稳态。某些菌株还能合成碱代谢物如氨,通过中和胞内酸性环境来增强生存能力。这种酸耐受性不仅使致龋微生物在恶劣环境中持续存活,还赋予其竞争优势——当环境pH降至临界值时,非致龋共生菌的生长受到抑制,而致龋菌仍能保持代谢活性。
微生物间的分子互作网络进一步放大了致龋效应。变异链球菌与乳酸杆菌(Lactobacillus)表现出明显的代谢协同性:前者产生的乳酸为后者提供碳源,而后者通过维持酸性环境促进前者的生态位占据。同时,某些放线菌属(Actinomyces)菌株可通过精氨酸脱氨酶系统产生碱性物质,这种代谢特性在健康状态下有助于缓冲酸性环境,但在龋病进程中可能被致龋菌群利用来调节局部pH波动,形成动态平衡的“酸性生态位”。
毒力因子的差异表达是决定微生物致龋潜能的核心因素。比较基因组学分析显示,高致龋性菌株通常携带更多编码黏附素、糖转运系统和应激反应蛋白的基因。这些基因的表达受到复杂调控网络的精细控制,包括双组分信号系统、小RNA调控以及表观遗传修饰等。例如,vicRK信号系统能同时调控生物膜形成、酸耐受性和多糖合成相关基因的表达,这种全局性调控模式使致龋微生物能够快速适应环境变化。
值得注意的是,近年研究发现某些传统认为的共生微生物如Scardovia wiggsiae在特定条件下也能表现出致龋特性。这些微生物通过独特的代谢途径如果糖磷酸激酶系统产生有机酸,或通过分泌蛋白酶降解唾液防御蛋白,间接促进致龋菌群的生态优势建立。这种发现拓展了对致龋微生物的认识范畴,提示龋病发生可能涉及更广泛的微生物功能网络而非单一病原体的作用。
3.2 宿主免疫反应与微生物组的互作
宿主免疫系统与口腔微生物组之间形成动态平衡关系,这种精细调控的互作网络对维持口腔健康至关重要。唾液作为口腔微环境的主要液体成分,其含有的多种免疫防御因子构成抵御致龋菌群的第一道防线。其中,分泌型免疫球蛋白A(sIgA)通过特异性结合微生物表面抗原,有效抑制变异链球菌等致龋微生物的黏附与定植。研究发现,健康个体唾液sIgA对致龋菌的表面黏附素表现出更高的亲和力,而在龋病活跃期,这种选择性抑制作用显著减弱,提示免疫识别效能的改变可能促进致病菌的生态位扩张。
先天免疫效应分子在调控微生物稳态中发挥多重作用。溶菌酶通过水解细菌细胞壁的肽聚糖层直接杀伤敏感菌群,而乳铁蛋白则通过螯合铁离子限制微生物的生长繁殖。值得注意的是,这些广谱抗菌物质的活性受局部微环境pH值影响显著——当口腔pH降至临界值时,其杀菌效能明显降低,这种特性与龋病发展过程中的酸性微环境形成恶性循环。此外,唾液中的组蛋白衍生肽如histatin-5对致龋菌生物膜形成具有特异性抑制作用,其分子机制涉及干扰微生物的群体感应信号传导通路。
口腔上皮细胞通过模式识别受体(PRRs)参与微生物组调控。Toll样受体(TLRs)和NOD样受体(NLRs)能够识别微生物相关分子模式(MAMPs),如脂磷壁酸和鞭毛蛋白,进而激活下游炎症信号通路。在健康状态下,这种识别反应维持在适度水平,通过调控防御素等抗菌肽的表达实现选择性微生物控制。然而,在龋病进程中,持续的酸性应激可导致上皮细胞TLR2/4表达异常,引发过度的炎症反应,这种改变不仅破坏局部组织稳态,还可能通过改变微环境促进耐酸菌群的增殖。
适应性免疫系统在微生物组调控中的作用日益受到关注。研究发现,龋病易感个体口腔黏膜中Th17细胞比例增加,其分泌的IL-17可刺激上皮细胞产生抗菌蛋白,但同时也会促进组织炎症反应。调节性T细胞(Treg)则通过分泌IL-10等抗炎因子维持免疫耐受,这种平衡的打破可能导致对共生菌群的异常攻击或对致龋菌的免疫逃逸。唾液中的IgG主要来源于牙龈沟液,其在龋病活跃期的滴度变化反映了系统性免疫应答的参与程度。
微生物组对宿主免疫系统的塑造作用同样不可忽视。特定共生菌如血链球菌能够诱导唾液sIgA的差异化分泌,这种选择性免疫应答有助于维持微生物群落平衡。某些放线菌属菌株则通过精氨酸脱氨酶系统产生氨,不仅中和局部酸性环境,还能调节宿主细胞的炎症反应强度。宏基因组关联分析显示,健康个体口腔微生物组中富含能够降解炎症介质的基因模块,这些功能基因可能通过减轻组织炎症反应间接抑制致龋菌的过度生长。
龋病发展过程中,免疫-微生物互作呈现明显的动态演变特征。早期阶段,宿主通过增强唾液分泌和防御蛋白表达试图恢复微生物平衡;随着病程进展,持续的酸性环境导致唾液缓冲能力下降,同时微生物生物膜结构限制免疫因子的渗透,形成免疫逃逸微环境。值得注意的是,某些代谢产物如短链脂肪酸在低浓度时可调节免疫细胞功能,但在高浓度下反而抑制中性粒细胞活性,这种浓度依赖性效应反映了宿主-微生物互作的复杂性。
潜在的治疗策略可针对免疫-微生物互作的关键节点进行干预。已有研究尝试通过局部应用sIgA增强剂或TLR激动剂来重建免疫防御屏障,而调节口腔pH值的缓释系统则可能恢复免疫因子的活性。对特定共生菌如血链球菌的定向增殖,或可增强其对致龋菌的竞争性抑制并刺激保护性免疫应答。这些干预措施的核心在于精准调控免疫系统与微生物组之间的对话,而非简单消除或抑制某一方,体现了从生态整体视角防治龋病的新思路。
第四章 研究结论与未来展望
本研究通过多组学整合分析,系统揭示了口腔微生物组在龋病发展中的动态变化规律及其分子互作机制。研究发现,龋病进程伴随着显著的微生物群落演替,变形菌门、放线菌门和厚壁菌门等核心菌群的结构变化与疾病阶段密切相关。致龋微生物通过糖酵解代谢网络增强产酸能力,协同群体感应系统调控的生物膜形成机制,共同驱动局部微环境酸化。值得注意的是,宿主免疫防御机制与微生物组之间形成的动态平衡被打破是龋病发生的关键环节,唾液防御蛋白功能抑制与特定菌群的免疫逃逸现象共同促进了致龋菌群的生态优势建立。
未来研究应从以下几个方向深入探索:首先,需要建立更精确的微生物功能网络模型,整合宏转录组和代谢组数据,阐明不同生态位微生物在龋病发生中的时空特异性作用。其次,针对微生物群体感应系统的干预策略值得重点关注,开发能够特异性干扰致龋菌群信号传导的小分子抑制剂可能成为新型防治手段。第三,应加强宿主遗传因素与微生物组互作的研究,通过全基因组关联分析鉴定影响个体龋病易感性的关键基因变异。此外,基于共生微生物的抗龋特性开发益生菌制剂或微生物移植疗法,可能为恢复口腔微生态平衡提供新思路。
技术方法层面,单细胞测序技术的应用将有助于解析致龋菌群的异质性及其在生物膜微环境中的功能分化。同时,发展原位检测技术如拉曼光谱结合稳定同位素标记,可实现口腔微生物代谢活动的实时可视化监测。跨学科研究应关注微生物组与口腔材料学的交叉领域,探索具有微生态调控功能的智能修复材料。
临床应用方面,未来需开展大规模人群队列研究,建立基于多组学特征的龋病风险预测模型,推动龋病防治向精准医学模式转变。同时,开发针对不同龋病阶段的个性化微生态调控方案,如靶向调节特定代谢通路或关键菌群的干预措施,将有望突破传统防治方法的局限性。这些研究方向的推进不仅将深化对龋病生态学机制的认识,也将为开发基于微生物组调控的创新防治策略奠定坚实基础。
参考文献
[1] 侯明.菌群微生物的多组学技术在儿童龋病研究中的应用[J].《实用口腔医学杂志》,2025,(2):283-288.
[2] 潘丽英.外泌体蛋白质组学在植物与微生物互作中的研究进展[J].《安徽农业科学》,2024,(16):13-19.
[3] 朱玉娟.常用分子检测技术在儿童龋病微生物多样性研究中的应用[J].《口腔医学研究》,2016,(2):202-206.
[4] 陈澍.硫代葡萄糖苷治疗炎症性肠病的作用机制研究[J].《天然产物研究与开发》,2025,(4):694-706.
[5] 霍媛媛(综述).龋病相关微生物群落结构与功能的多组学研究进展[J].《口腔疾病防治》,2018,(3):195-199.
[6] 苏志飞.口腔微生物宏转录组在口腔疾病中的研究进展[J].《口腔医学研究》,2020,(8):716-718.
[7] 程赛赛.生态进化视角的植物-微生物组互作研究进展[J].《生物技术通报》,2020,(9):3-13.
[8] 李海斌.基于外周血单个核细胞转录组测序结果的硅沉着病发病机制研究[J].《郑州大学学报(医学版)》,2024,(6):782-787.
[9] 富饶.口腔微生物共聚的研究进展[J].《国外医学(口腔医学分册)》,2003,(5):346-348.
[10] 朱彦.口腔微生物生物膜分散物质的研究进展[J].《华西口腔医学杂志》,2014,(6):625-630.
[11] 艾超.植物根际沉积与土壤微生物关系研究进展[J].《植物营养与肥料学报》,2015,(5):1343-1351.
[12] 范宇.吸烟影响口腔微环境及其在龋病进展中的作用[J].《国际口腔医学杂志》,2021,(5):609-613.
[13] 刘诗雨.白假丝酵母菌与龋病的相关性及其致龋机制[J].《国际口腔医学杂志》,2017,(1):103-107.
[14] 梁潇月.口腔疾病与抑郁症的关系[J].《口腔疾病防治》,2024,(8):625-631.
[15] 王欣妍.游离糖与龋病关系的研究进展[J].《口腔疾病防治》,2023,(11):813-818.
[16] 杨晓琼.低龄儿童龋与其相关致病菌的研究进展[J].《国际口腔医学杂志》,2011,(4):455-459.
[17] 罗瑜雪.韦荣球菌与口腔疾病的研究进展[J].《华西口腔医学杂志》,2020,(5):576-582.
[18] 陈晖.克罗恩病胆汁酸代谢靶点基因筛选及在疾病诊断和治疗监测中的价值[J].《中国组织工程研究》,2025,(32):7028-7040.
[19] 许萌萌.互作转录组测序技术在微生物研究中的应用进展[J].《四川大学学报(医学版)》,2022,(2):201-207.
[20] 周学东.人类口腔微生物组学研究:现状、挑战及机遇[J].《微生物学报》,2017,(6):806-821.
通过以上口腔毕业论文写作指南及范文解析的系统梳理,我们已为您拆解了选题定位、结构搭建与数据分析等核心环节。掌握这些写作方法论,不仅能提升论文质量,更能培养严谨的科研思维,为未来口腔医学领域的学术研究奠定坚实基础。



